溶液 の 質量 の 求め 方 217773

モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ
物質量の求め方を紹介してみました。 単位はmol(モル)でこれは 分子量60×10 23 を示したものです。 molの計算問題のポイントは、molから求める時はかけ算、molを求めるなら割り算に 質量分率は、溶液の全質量に対するこの成分の質量の比として計算されます。 結果をパーセントで取得するには、結果の商に100を掛ける必要があります。 式は次のようになります。 m = m(溶質)/ m(解) %、%= 100 * 2
溶液 の 質量 の 求め 方
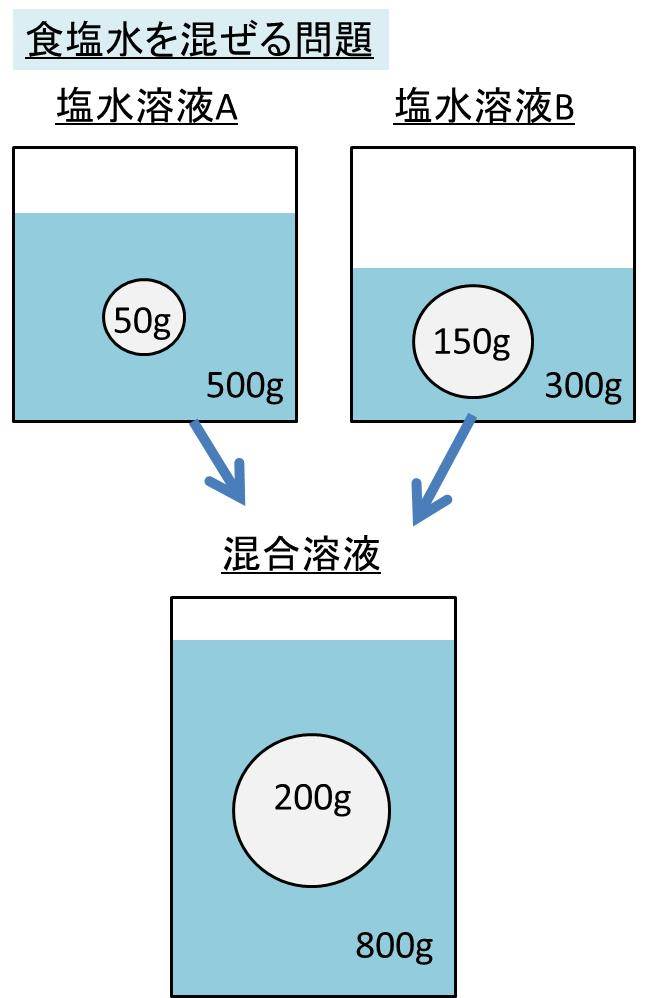
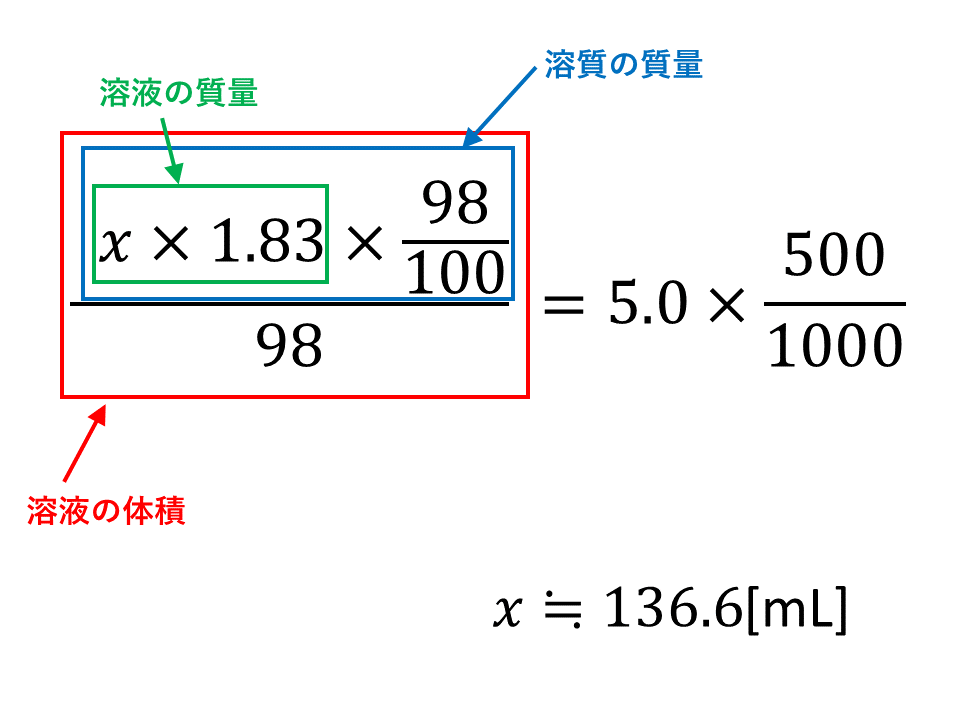
溶液 の 質量 の 求め 方- 混合溶液の体積の和を計算で求めることは不可能です。 一般に、2種類の溶液を混合すると体積が減りますが、これは分子の形状や 水素結合の有無に影響しますので、計算できるものではありません。 やってみるしかないのです。1 溶液の濃度とその表し方 5 9808g/mol 1,803g =18mol この物質量のH2SO4が1Lに含まれているので硫酸の容量モル濃度は184mol/L。 ② 酢酸1Lの重さは1,050gで,100%酢酸中の酢酸の質量は

4 6 溶液の濃度 おのれー Note
なお,この溶液の質量は 11 kg である。9 wt %の塩化ナトリウム水の密度(25℃)約 1061 kg / m 3 から,25 ℃での溶液の体積は,11 / 1061 = m 3 = 1037 L と計算される。PH値の求め方|基礎講座|技術情報・便利ツール|株式会社タクミナ 基礎講座|pH中和処理制御技術 23 pHとは? pH値の求め方 少し数学的に表現するとpHは、つぎのように定義されます。 pH =-logH logとは、対数(ロガリズム)のことで、x=10 n の 説明 モル濃度、溶質の分子量(式量)、溶液の密度から、質量パーセント濃度を自動的に計算するツールです。 使い方 モル濃度が1、 密度1g/cm3 の希塩酸(HClの分子量は365)の質量パーセント濃度を求め
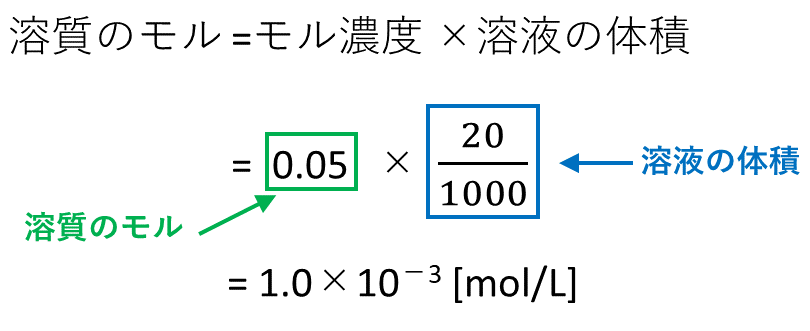
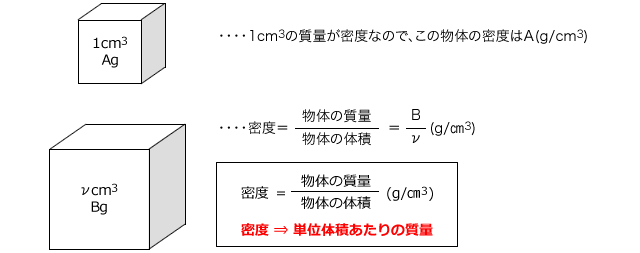
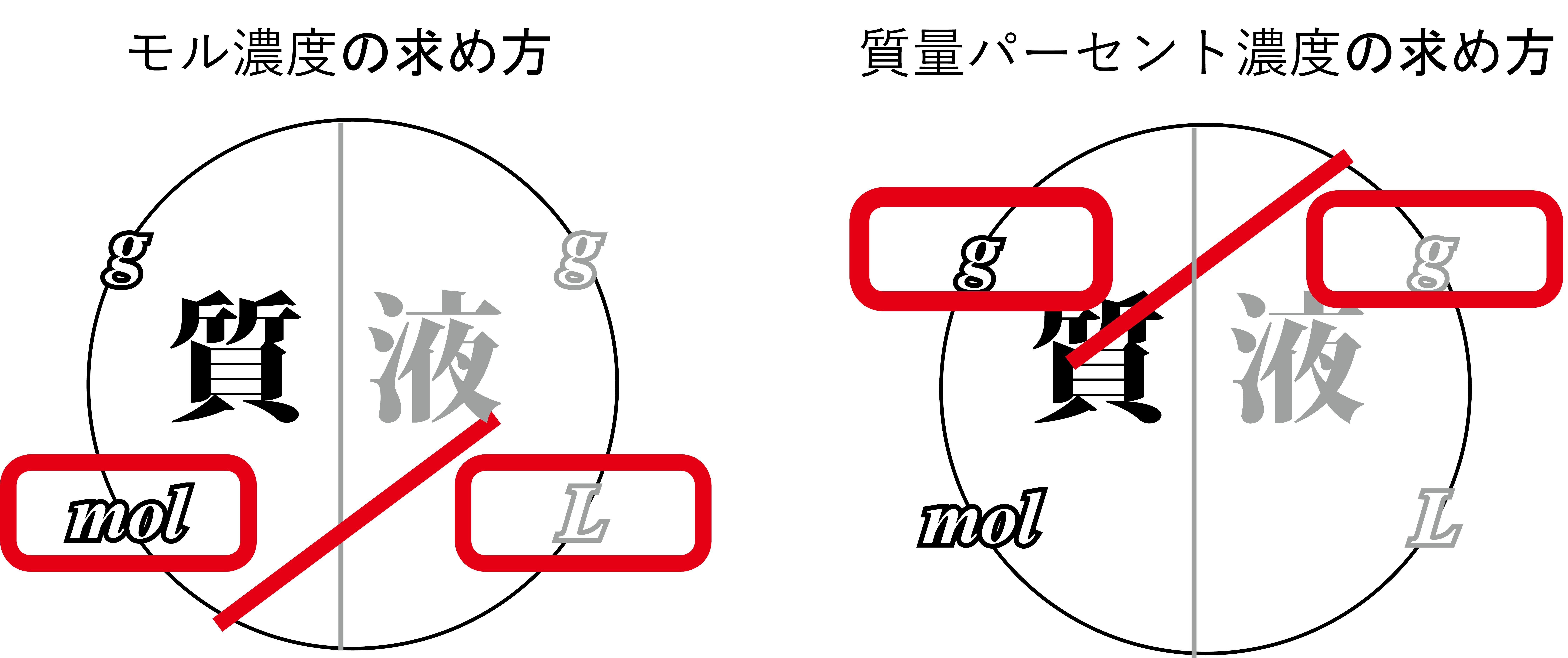
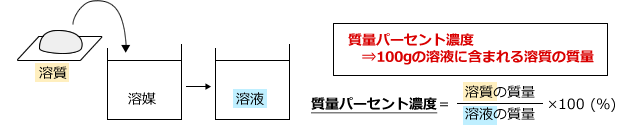
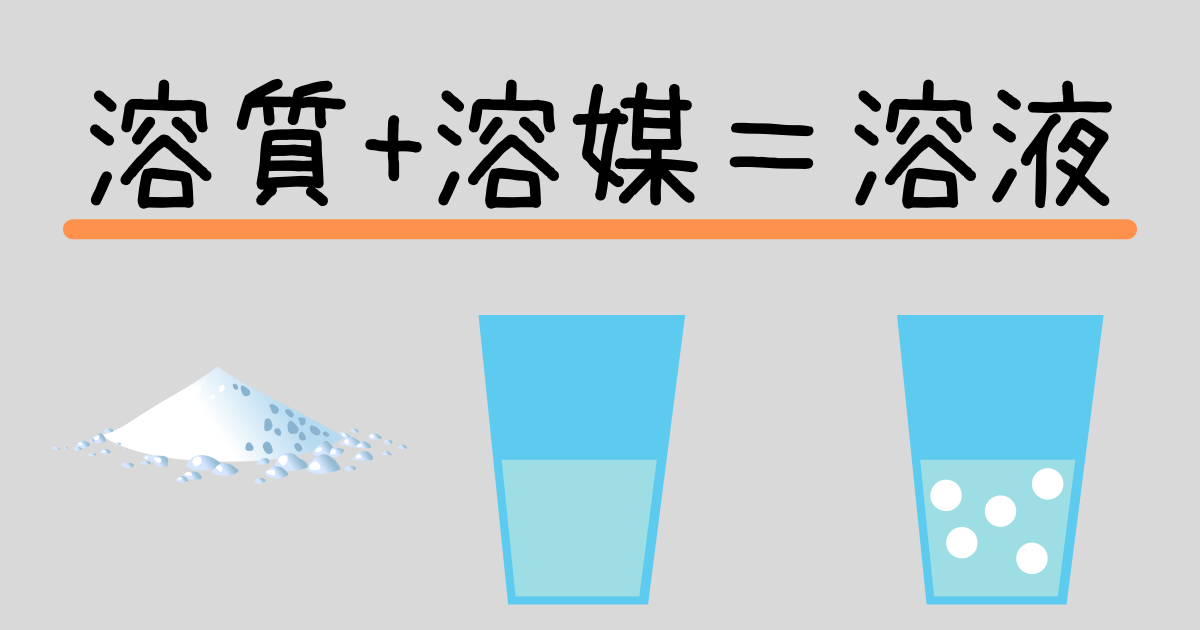
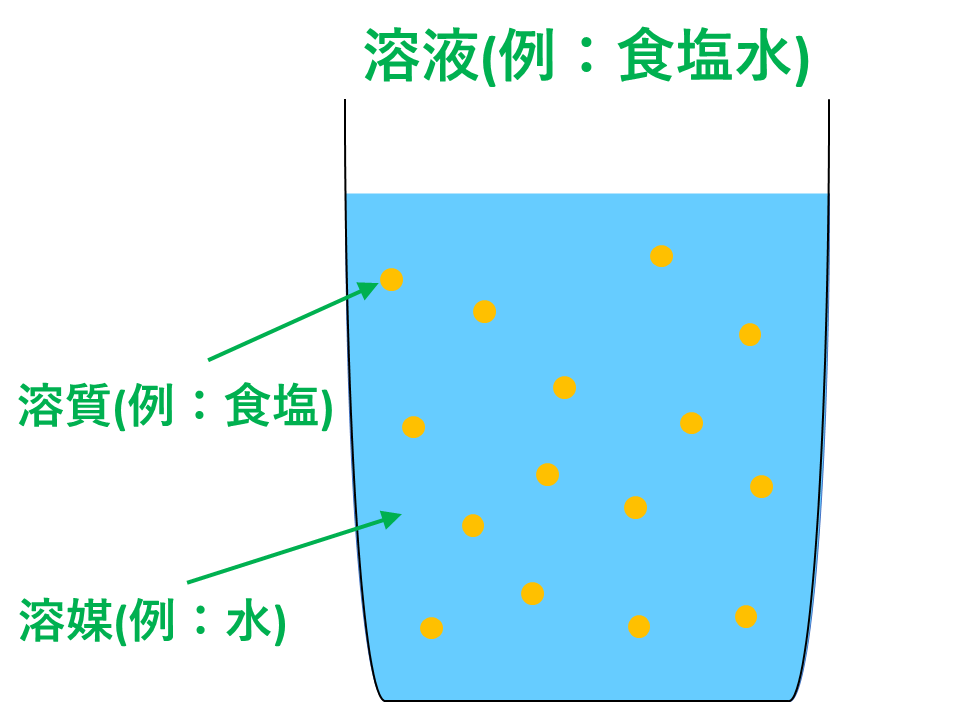
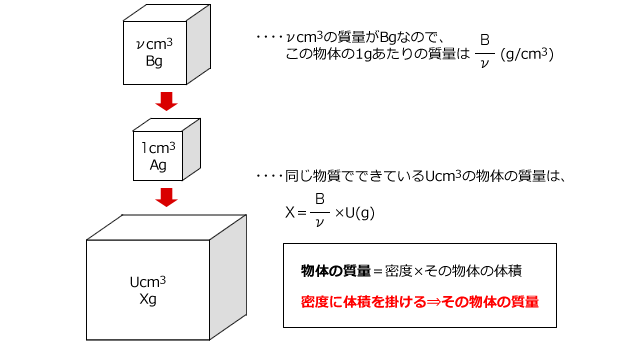
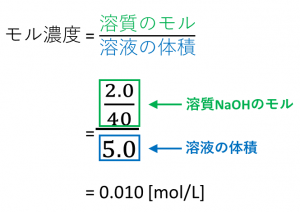
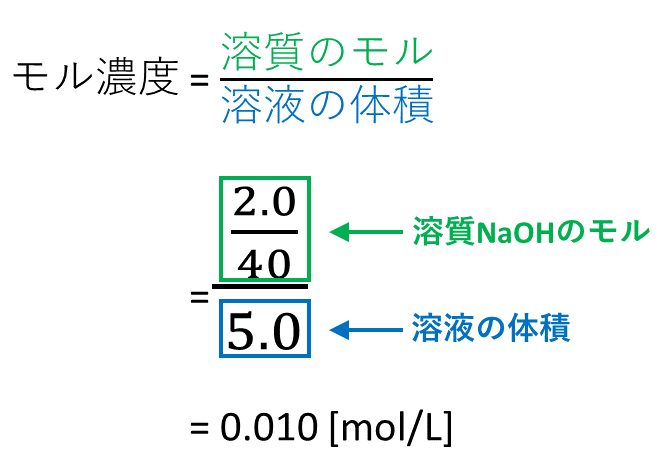
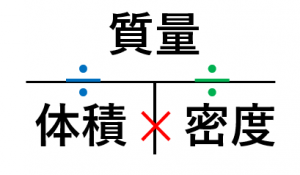
モル濃度とは 溶質の物質量molを溶液の体積Lで割ったもの である。 上の式はモル濃度を求める公式として知られており、しっかりと暗記しておく必要がある。 ちなみに、溶液・溶質というのがそれぞれ何を指すのかは正確に理解しておこう。 密度の求め方や周辺の測定実験なども含めて他の分野との複合問題として出題されることもあります。 密度 とは,物体の質量 より溶液の重さは5gと計算しているので,これを溶液の密度093g/cm 3 で割ると,5÷093=9623≒962より溶液の体積は962cm 3はじめに ここでは、溶液の濃度を表す単位である質量パーセント濃度、モル濃度そして質量モル濃度の単位、求め方についてまとめています。 質量パーセント濃度 小学校や中学校で、食塩水の濃度を求めてみましょうという問題を解いたのを記憶しれいる人も多いかと
溶液 の 質量 の 求め 方のギャラリー
各画像をクリックすると、ダウンロードまたは拡大表示できます
 |  |  |
 |  |  |
 |  |  |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  |  |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  |  |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  |  |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  |  |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 | ||
 |  |  |
 |  |  |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  | |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
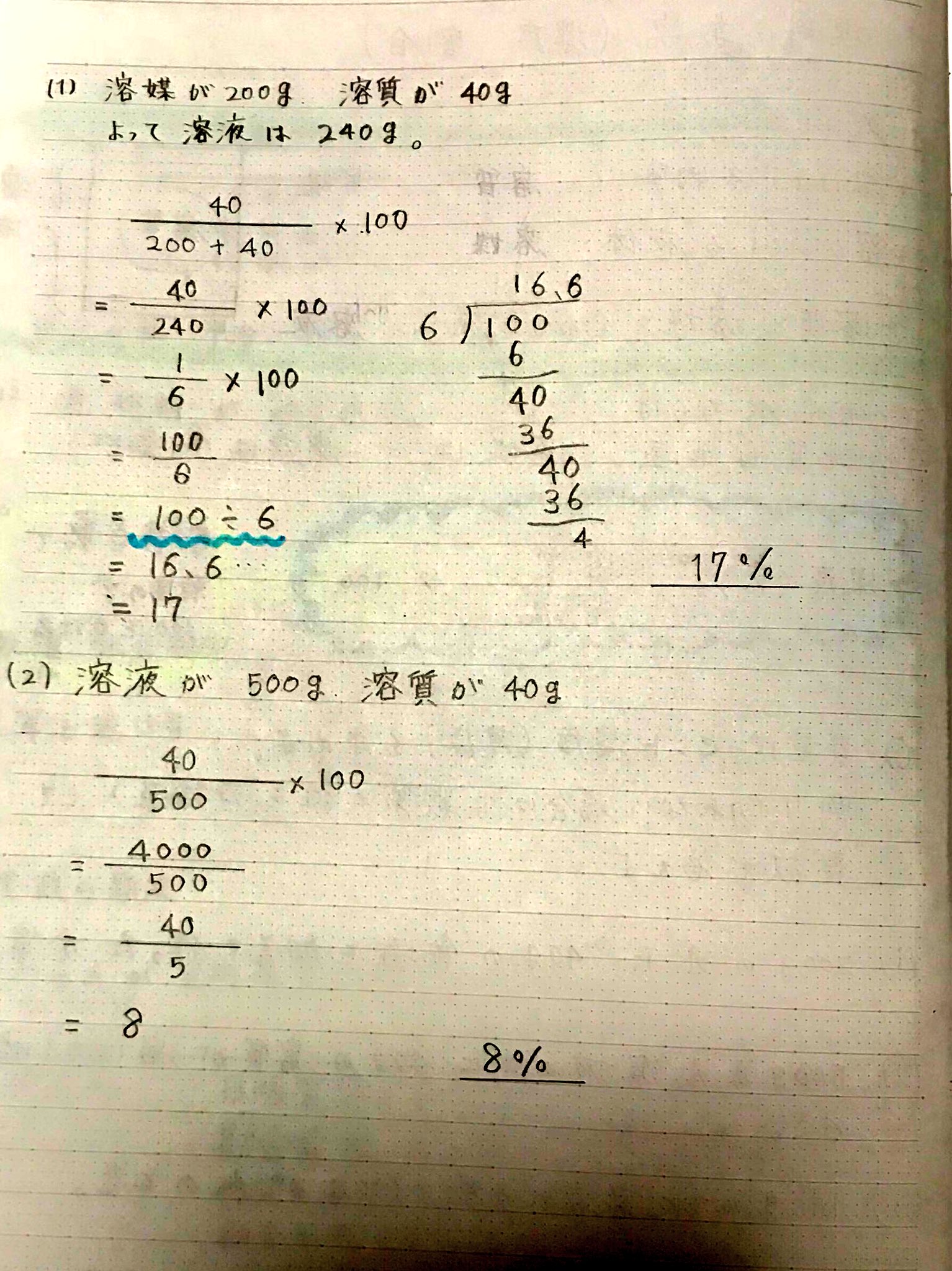 |  |  |
 |  |  |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |  |  |
 |  |  |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  |  |
 |  | |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  |  |
 |  | |
 |  |  |
「溶液 の 質量 の 求め 方」の画像ギャラリー、詳細は各画像をクリックしてください。
 |  | |
 |
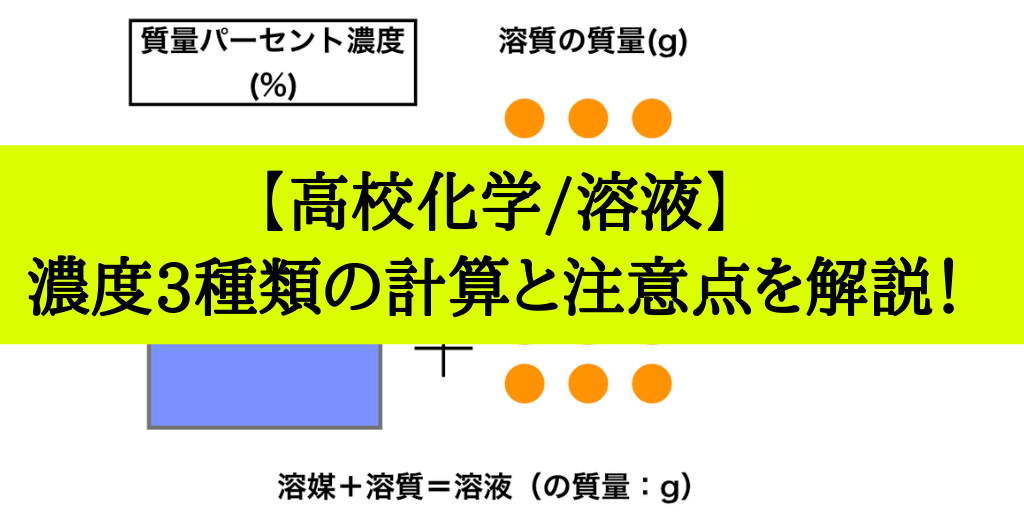
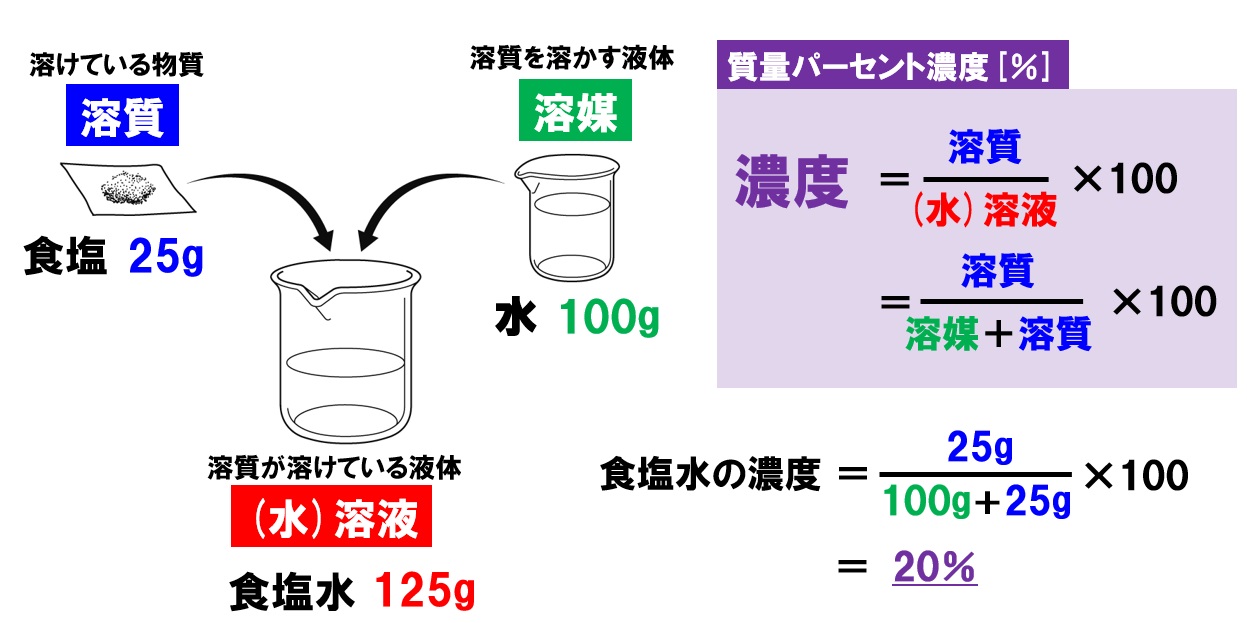
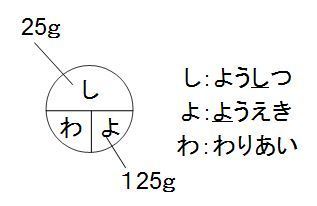
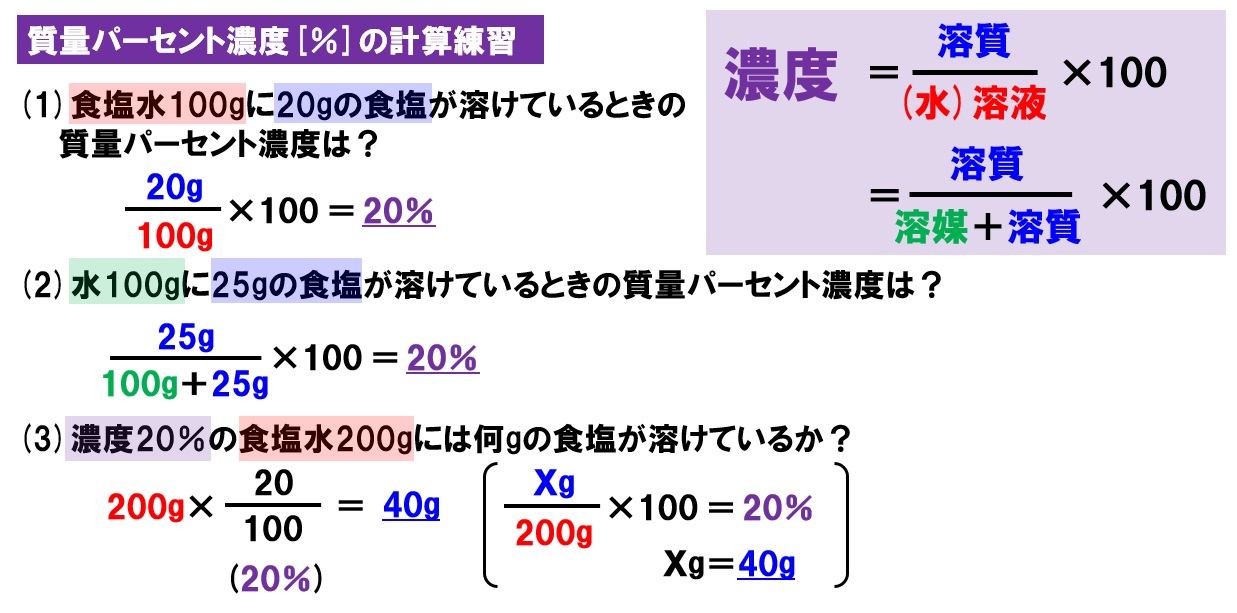
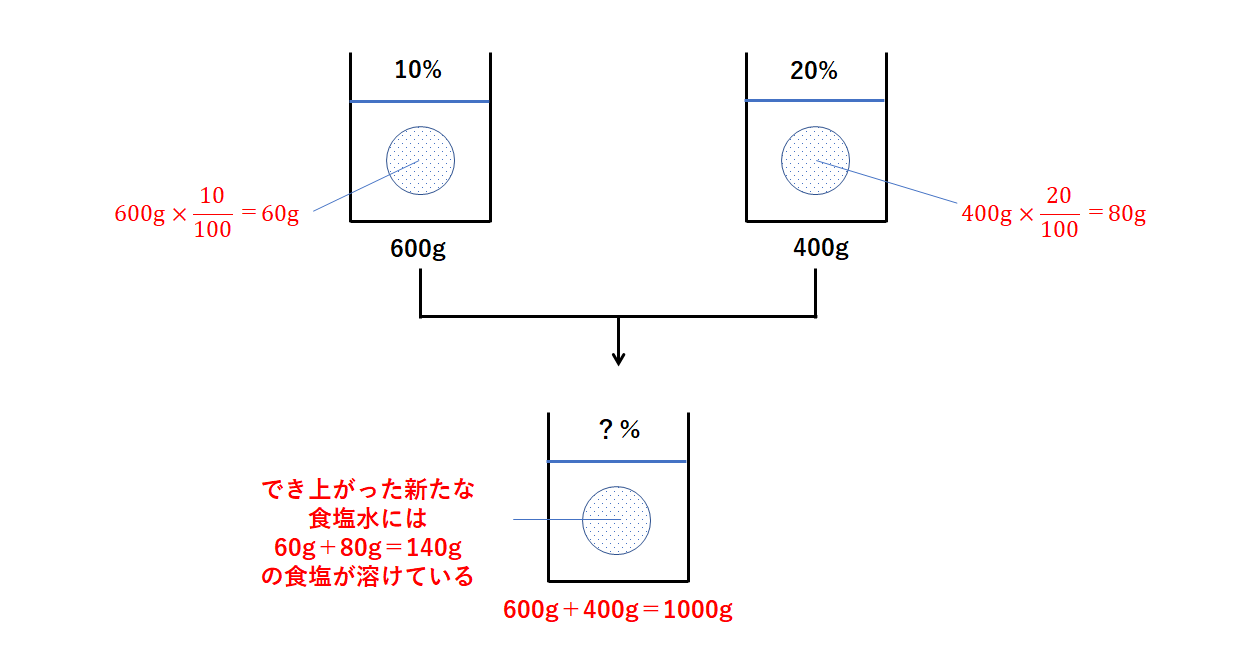
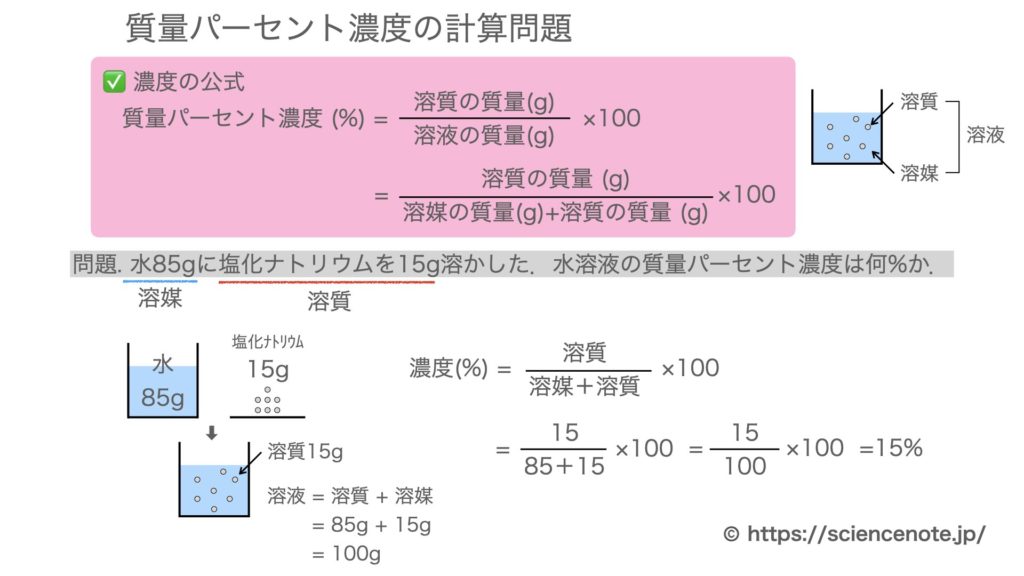
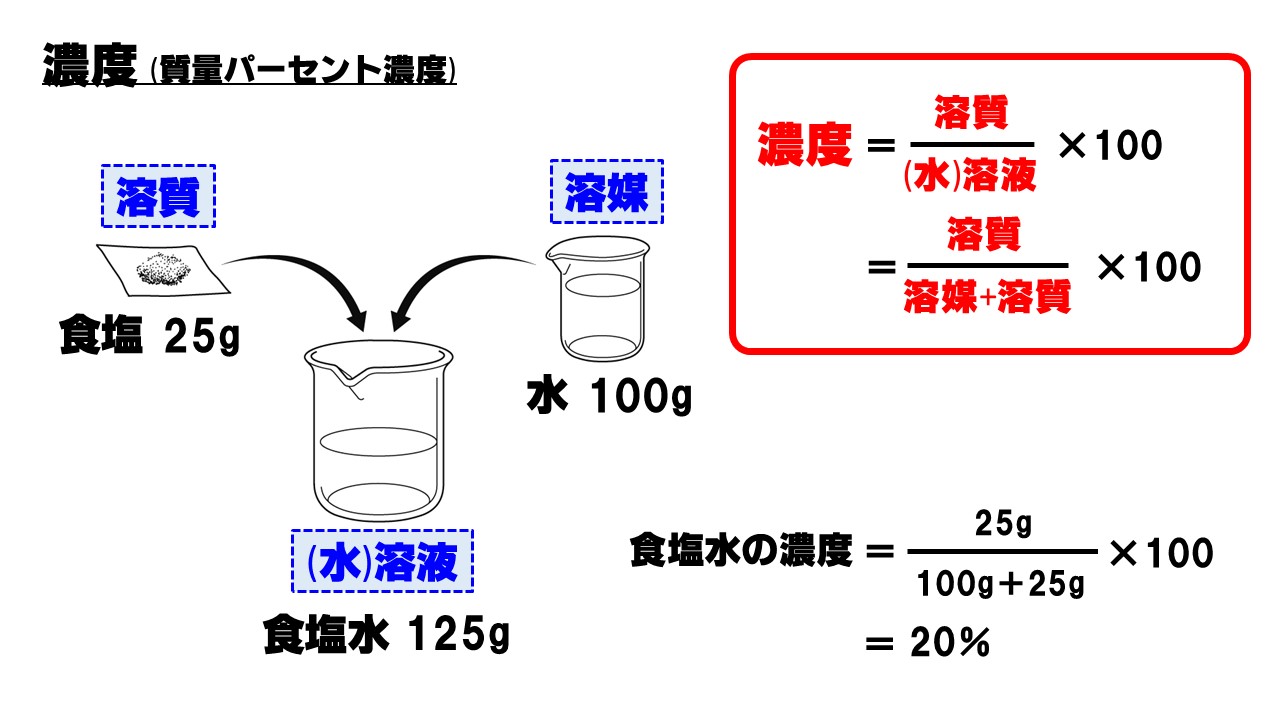
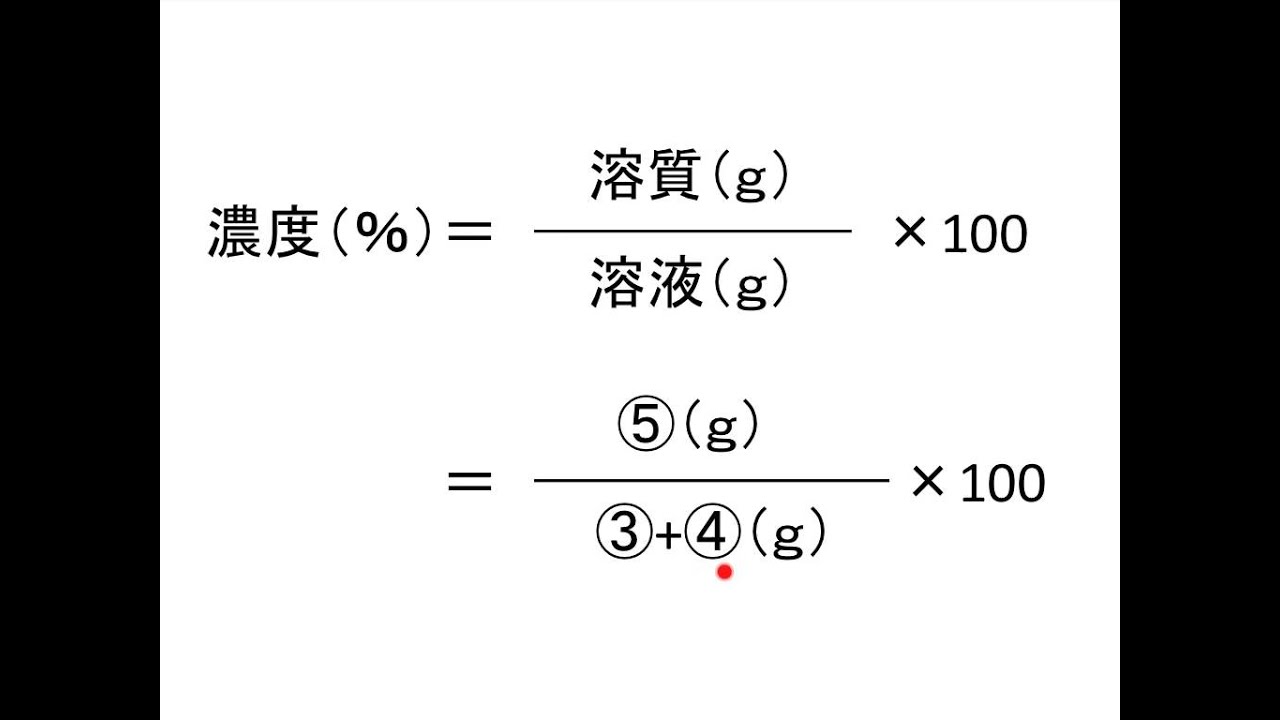
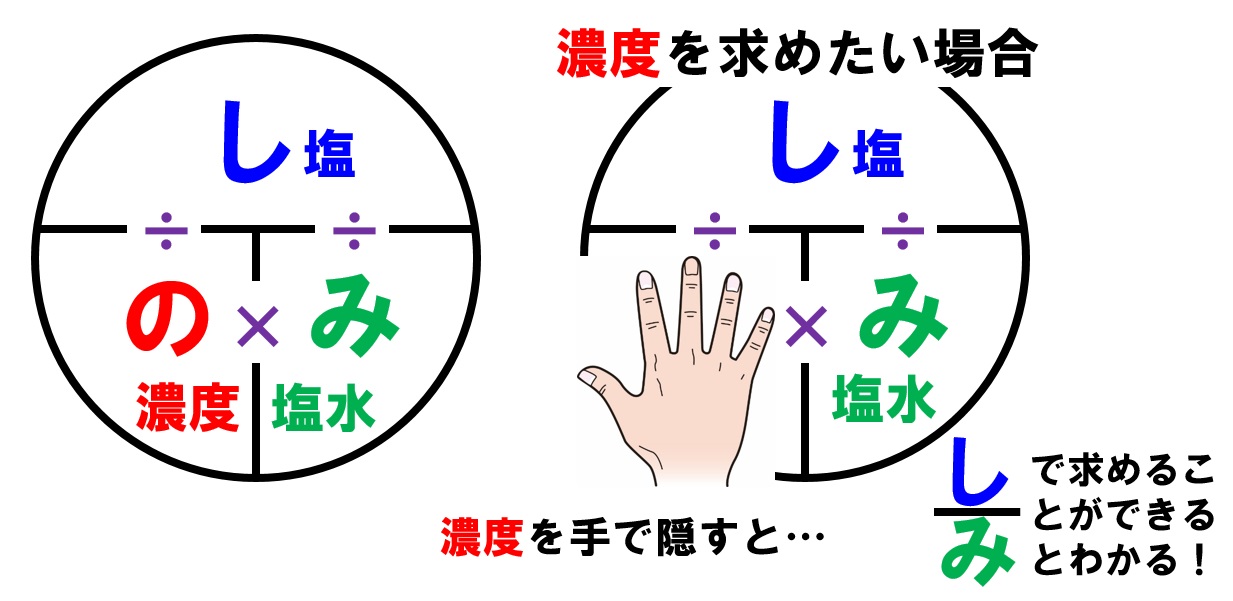
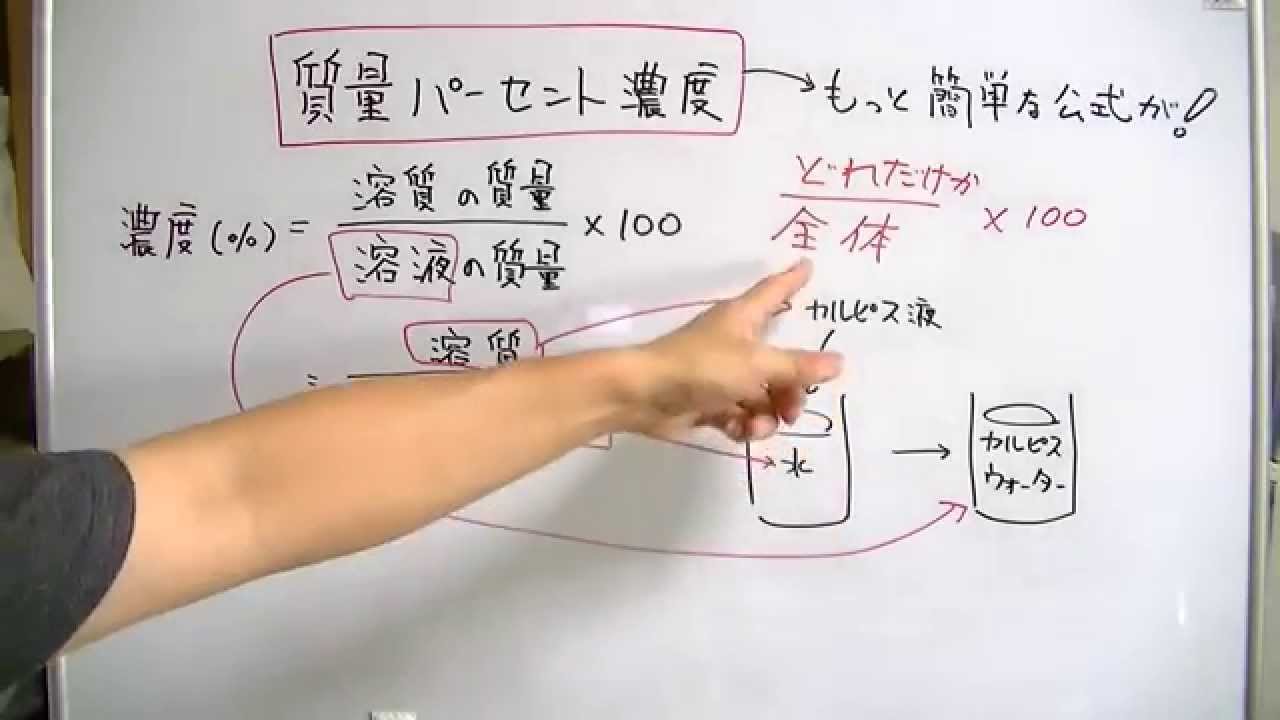
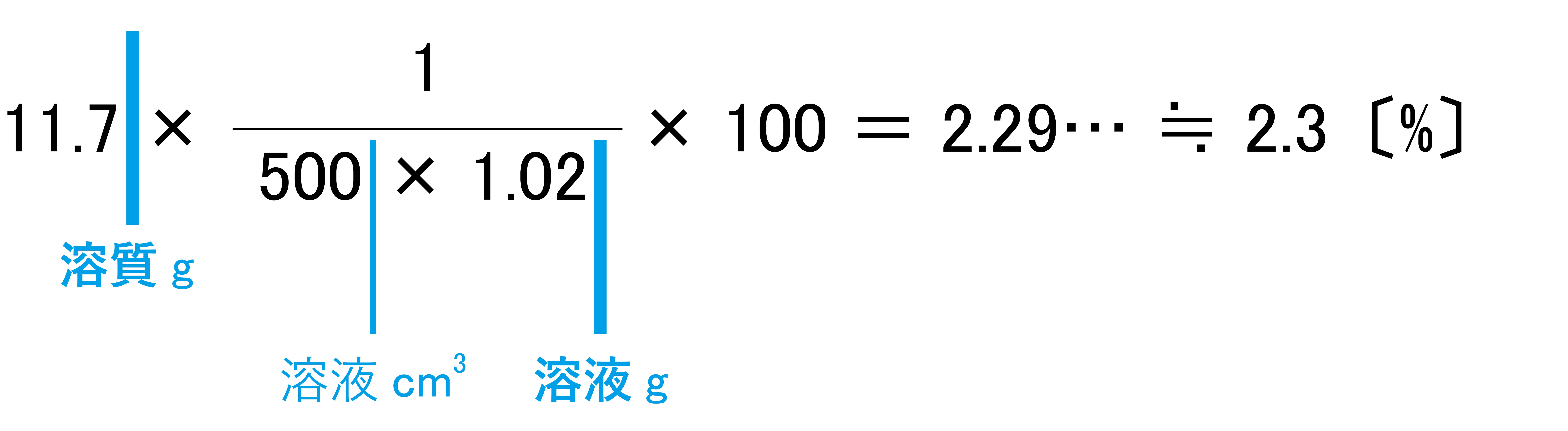
星の王子 さん 水より重い液体に適用される式です。 d = 1443/(1443 - Bh) d : 15℃水溶液の 比重(4℃の水を規準として) Bh : 15℃水溶液の ボーメ度 この式は元々 実験式ですし、また式の成り立ちから見ても計算結果の有効数字は 3桁か、せいぜい 4桁 と考えるべきです。最初に触れましたが、質量パーセント濃度は以下の式で求められます。 質量パーセント濃度(%)= 溶質の質量(g)÷ 溶液(溶質溶媒)の質量(g)×100 これは、溶液の中に溶けている溶質が全体の何パーセントかということです。





コメント
コメントを投稿